AMRN
Etilo de icosapento: un tratamiento exitoso para la infección sintomática por COVID-19
DOI: 10.7759 / cureus.10211
Cite este artículo como: Berger AA, Sherburne R, Urits I, et al. (02 de septiembre de 2020) Icosapent Ethyl: un tratamiento exitoso para la infección sintomática por COVID-19. Cureus 12 (9): e10211. doi: 10.7759 / cureus.10211
Resumen
COVID-19 es una pandemia fatal y universal causada por el virus SARS-CoV-2 que ha causado directamente al menos 95,235 muertes en los EE. UU. En mayo de 2020. Tiene un pronóstico desfavorable con una tasa de mortalidad de hasta el 21% en general. población en el apogeo de la pandemia, una tasa que es mucho mayor en los pacientes ancianos, así como en aquellos que requieren cuidados en la unidad de cuidados intensivos (UCI). Se está estudiando el papel de la inflamación en el COVID-19 sintomático y se plantea la hipótesis de que la hiperinflamación es un factor causante de la enfermedad grave del COVID-19. Las opciones de tratamiento son limitadas y se basan principalmente en cuidados de apoyo.
El etilo de icosapent (IPE) es un derivado de ácidos grasos omega-3 que ha demostrado reducir significativamente la mortalidad cardiovascular y se utiliza como complemento de la terapia con estatinas. Aunque se ha demostrado que actúa como antiinflamatorio, actualmente no está indicado para ese propósito. Aquí, describimos, por primera vez, el tratamiento exitoso de un paciente con COVID-19 con EPI.
Introducción
COVID-19 es una pandemia fatal y universal. Originario de Wuhan, la capital de la provincia de Hubei en China, es causado por el virus SARS-CoV-2 (anteriormente 2019-nCov), que se transmite eficientemente de persona a persona. Con mayor frecuencia, causa una enfermedad respiratoria que podría deteriorarse hasta convertirse en síndrome de dificultad respiratoria del adulto (SDRA)
[1-2] . Se informa que la mortalidad global por COVID-19 oscila entre el 2,1% y el 21%
[2-5] , con una vulnerabilidad específica en pacientes mayores de 70 años
[3] . En los Estados Unidos, se estima que causó directamente 95.235 (de un exceso de 122.300) muertes entre marzo y mayo de 2020
[6].. En los pacientes que requieren cuidados en la unidad de cuidados intensivos (UCI), intubación y ventilación, el pronóstico es aún peor y solo una pequeña fracción sobrevive
[3,5,7] .
Se ha planteado la hipótesis de que la inflamación juega un papel causal en el COVID-19 sintomático y la evidencia apunta a estados hiperinflamatorios en los pacientes
[5] . Esto está respaldado por los resultados preliminares del ensayo de evaluación aleatoria de la terapia COVID-19 (RECOVERY; NCT04381936)
[8] y la incorporación de la dexametasona en las directrices de tratamiento de los Institutos Nacionales de Salud (NIH)
[9] . Desafortunadamente, fuera de la dexametasona, las opciones de tratamiento para COVID-19 son muy limitadas. Se pensaba que los medicamentos contra la malaria, cloroquina e hidroxicloroquina, brindaban cierta protección contra la propagación viral. Sin embargo, evidencia reciente sugiere que es posible que no confieran la defensa que se pensaba anteriormente
[4].. También se estudió el tratamiento con tocilizumab, pero la bibliografía sobre los inhibidores de IL-6 no es concluyente
[10-11] . El tratamiento principal para COVID-19 sigue siendo principalmente de apoyo.
El etilo de icosapento (IPE), una forma de ácido eicosapentaenoico (EPA), está indicado para el tratamiento de la hipertrigliceridemia persistente, ha demostrado reducir el riesgo cardiovascular y se ha informado que tiene actividad antiinflamatoria
[12] . Actualmente está indicado como complemento de la terapia con estatinas máximamente tolerada
[13-15] . Dado que el efecto reductor de triglicéridos de la EIP fue solo modesto, el mecanismo de reducción del riesgo cardiovascular aún no está claro. Un mecanismo sugerido es el efecto antiinflamatorio de IPE
[16].. Esto está respaldado por los resultados de la Evaluación del efecto de dos dosis de AMR101 (icosapentato de etilo) sobre los niveles de triglicéridos séricos en ayunas en pacientes con niveles altos persistentes de triglicéridos (≥ 200 mg / dL y <500 mg / dL) a pesar de la terapia con estatinas (ANCHOR ; NCT01047501) y el estudio multicéntrico, controlado con PlAcebo, aleatorizado, doble ciego, de 12 semanas con un ensayo de extensión abierta (MARINE; NCT01047683), que muestra una reducción de los marcadores inflamatorios en pacientes en tratamiento con EPI
[17- 19] . Actualmente, el IPE no está indicado para el tratamiento antiinflamatorio. Aquí, informamos, por primera vez, el uso de IPE para tratar a un paciente con COVID-19.
Presentación del caso
Una mujer de 53 años (paciente n. ° 1) con hiperlipidemia y ninguna otra afección médica conocida se presentó a la clínica después de una exposición confirmada, así como una prueba positiva para COVID-19. Su hija sana de 21 años (paciente n. ° 2) estuvo igualmente expuesta al mismo tiempo. Ambas mujeres gozaban de buena salud, no tenían otros factores de riesgo conocidos de COVID-19 y tenían un índice de masa corporal (IMC) de 21 y 17, respectivamente. No habían mostrado ningún síntoma y no recibieron tratamiento hasta el cuarto día posterior a la exposición. Cuatro días después de haber sido expuestos a un caso confirmado de COVID-19, ambos desarrollaron fiebres persistentes hasta 101F y posteriormente dolor de garganta, congestión nasal y tos en el día de los síntomas (SD) 2 y anosmia en SD4. En SD2, después de obtener el consentimiento informado, el Paciente # 1 comenzó un curso de IPE oral (2 g dos veces al día). Este tratamiento se le ofreció después de nuestro éxito con este régimen en pacientes con respuesta inflamatoria y shock (informe en revisión para publicación). Su hija (paciente n. ° 2) rechazó la IPE. Por lo demás, solo recibieron atención sintomática que no difirió entre los dos.
La fiebre comenzó a disminuir en SD2, sin embargo, los síntomas persistieron; en SD4, el paciente de 53 años ya no refirió ningún síntoma fuera de la anosmia, que luego se resolvió en SD7, cinco días después de comenzar el tratamiento con IPE. En comparación, su hija de 21 años continuó experimentando dolor de garganta, congestión nasal y anosmia a través de SD18. Solo había comenzado a experimentar un alivio parcial en SD18, significativamente después de la resolución completa de los síntomas en su madre (ver líneas verticales rojas en la Figura
1 ). La Figura
1 muestra el curso de la enfermedad en ambos pacientes y enfatiza la diferencia en el desarrollo de la enfermedad con y sin tratamiento IPE.
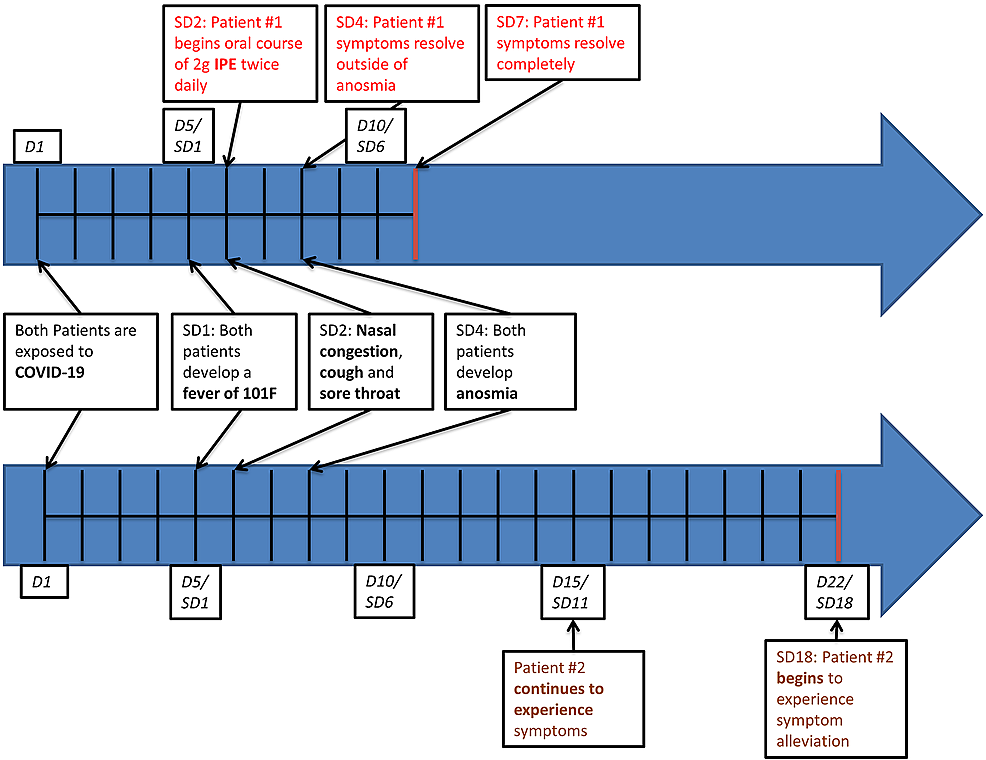
Figura 1: Cronología del desarrollo y alivio de los síntomas
La línea de tiempo resume el curso de la enfermedad en nuestros dos pacientes. El paciente n. ° 1 eligió comenzar la terapia IPE; su hija (Paciente # 2) optó por no participar en la terapia de EIP. Dentro de los cinco días posteriores al inicio de la terapia IPE, el Paciente # 1 se convirtió y permaneció libre de síntomas de COVID-19. Su hija continuó experimentando síntomas que solo comenzaron a disminuir en SD18.
D, día; SD: día del síntoma; IPE, etilo de icosapento
Discusión
Estos son dos pacientes con antecedentes genéticos y médicos similares que difieren solo en la edad y ninguno de los dos se consideraría anciano. Fueron expuestos de la misma manera al COVID-19, desarrollaron síntomas similares, pero solo uno fue tratado con IPE y experimentó síntomas de duración mucho más corta. Sorprendentemente, y en contraste con nuestro conocimiento sobre el COVID-19 hasta ahora, al paciente mayor le fue mejor. Estos casos moderados de COVID-19 se suman a nuestra experiencia previa con pacientes graves, hipóxicos de COVID-19 y sépticos (serie de casos de otros tres pacientes graves de COVID-19 aún no publicada, informe de caso para el uso de IPE en pancreatitis grave actualmente en revisión), lo que demuestra la utilidad de la EPI en estados inflamatorios agudos y específicamente con infecciones por COVID-19.
En el ensayo IPE Reduction of Cardiovascular Events with EPA-Intervention (REDUCE-IT; NCT1492361) diseñado para determinar la reducción del riesgo de enfermedad cardiovascular, la disminución de los triglicéridos fue modesta, lo que sugiere que los mecanismos IPE incluyen un efecto antiinflamatorio. Esto está respaldado por la evidencia de una reducción significativa de los marcadores inflamatorios con el uso de IPE en los ensayos ANCHOR y MARINE, que fueron diseñados para evaluar la actividad reductora de triglicéridos de IPE, así como por evidencia previa de ensayos de la EPA
[12] . La modulación inmunitaria es la acción más probable de la EPI en nuestros pacientes; sin embargo, también se informó anteriormente que la EIP y la EPA mejoran la función endotelial y tienen actividad virucida directa
[20].. Aunque el paciente n. ° 1 tenía antecedentes médicos de hiperlipidemia, es menos probable que se demuestren los efectos anti-lípidos en tan poco tiempo. Es probable que la investigación adicional en grupos más grandes de pacientes contribuya más a nuestra comprensión del mecanismo de acción subyacente.
Conclusiones
Aunque es anecdótico, presentamos la primera evidencia del uso de EPI como tratamiento para los síntomas asociados con una infección por COVID-19. Se requiere más investigación para explorar más a fondo la eficacia de IPE como tratamiento para COVID-19. Nuestro informe tiene como objetivo informar el tratamiento exitoso de COVID-19 con IPE en un solo caso con la esperanza de iniciar dicha investigación.